土壤基因组DNA提取试剂盒
|
货号
|
产品名称
|
规格
|
|
RTG2403
|
土壤基因组DNA提取试剂盒
|
50次
|
● 试剂盒内容及保存:
|
试剂盒组成
|
RTG2403(50次)
|
贮存方式
|
|
缓冲液R1
|
40
ml
|
常温
|
|
缓冲液R2
|
6
ml
|
常温
|
|
缓冲液R3
|
6 ml
|
常温
|
|
缓冲液R4
|
10
ml
|
常温
|
|
缓冲液 R5(浓缩液)
|
15
ml
|
常温
|
|
漂洗缓冲液WB1(浓缩液)
|
14
ml
|
常温
|
|
漂洗缓冲液PW (浓缩液)
|
13
ml
|
常温
|
|
洗脱液EB
|
15
ml
|
常温
|
|
Glass
beads
|
20 g
|
常温
|
|
吸附柱CG
|
50个
|
常温
|
|
收集管(2
ml)
|
50个
|
常温
|
|
说明书
|
1份
|
|
● 储存条件和效期:
本试剂盒在室温(25℃左右)干燥条件下,可保存1年。缓冲液R2和R3可能有沉淀产生,若溶液产生沉淀,应在使用前置于37℃下溶解沉淀至溶液澄清后再使用。
● 产品简介:
土壤样品存在大量的抑制因子如腐殖酸、金属离子等,而纯化的DNA 中只要有这些微量物质的存在,都会影响到PCR等酶促反应。本公司的土壤试剂盒采用独特的腐殖酸去除液(缓冲液R2)能够有效去除腐殖酸;吸附柱CG能能有效去除金属等抑制因子,提纯得到的基因组DNA可直接用于PCR
反应,酶切或定量实验。
● 准备工作:
1. 准备55℃,70℃水浴;无水乙醇;异丙醇;制冰机;1.5ml离心管;2ml离心管
2. 按照标签所示在漂洗缓冲液WB1和漂洗缓冲液PW中加入无水乙醇;缓冲液R5中加入异丙醇,混匀后盖紧瓶盖后室温贮存备用。
3. 每次使用前请检查缓冲液R2,缓冲液R3是否有沉淀生成,如果出现沉淀,37℃温浴至沉淀溶解后再使用。
● 标准操作步骤:
如非指出,所有离心步骤均为使用台式离心机在室温下离心。
1. 称0.3-0.5 g土壤置于2ml离心管中,加入0.4gGlass Beads,再加入700 μl 缓冲液R1与100
μl 缓冲液R2。涡旋器高速震荡3-5min。
注意:对含水量丰富的样品,可以预先离心除去部分水分后再称取样品。缓冲液R2是腐殖酸去除剂,100μl对大部分样品来说足以有效除去腐殖酸等抑制因子。对一些腐殖酸含量特别丰富的土壤, 缓冲液R2的量可以适当增加,但不能超过250μl,否则会严重影响DNA的得率。
2. 加入100
μl 缓冲液R3(R3如有沉淀37℃水浴完全溶解后再用),涡旋混匀。70℃水浴处理10min。期间振荡几次。注意:如果要纯化革兰氏阳性菌的DNA,请在70℃处理完后,再90℃水浴处理2min。
3. 12000 rpm(~13,000g)离心1分钟,取600μl上清到1.5ml离心管中,加入180 μl 缓冲液R4混匀。
注:转移上清时确保不要吸取到沉淀,转移的上清量最好不超过80%。
4. 冰上放置5分钟。12000 rpm(~13,000g)离心1分钟。
转移上清到新的1.5ml离心管中。
注:转移上清时确保不要吸取到沉淀,转移的上清量最好不超过80%。
5. 加入与上清等体积的缓冲液R5(使用前请检查是否已加入异丙醇),颠倒混匀。
6. 取750 μl混合液加到吸附柱中(吸附柱放入收集管中),12000 rpm(~13,000g)离心30秒,倒掉滤出液。
7. 将剩余混合液加到吸附柱中(吸附柱放入收集管中),12000rpm(~13,000g)离心30秒,倒掉滤过液。
8. 向吸附柱CG中加入500
μl 漂洗缓冲液WB1(使用前请先检查是否已加入无水乙醇),12,000
rpm (~13,000×g ) 离心30
秒,倒掉废液。
9. 向吸附柱CG中加入600
μl 漂洗缓冲液PW(使用前请先检查是否已加入无水乙醇),12,000
rpm (~13,000g) 离心30
秒,倒掉废液,吸附柱CG放入收集管中。
10. 向吸附柱CG中加入600
μl漂洗缓冲液PW,12,000
rpm (~13,000g) 离心30秒,倒掉废液,将吸附柱CG放入收集管中。
11. 12,000 rpm(~13,000g)离心2分钟,以彻底晾干吸附材料中残余的漂洗液。
注:此步骤非常重要,其目的是将吸附柱中残余的漂洗液去除。漂洗液中乙醇的残留会影响后续的酶反应(酶切、PCR等)实验。
12. 将吸附柱CG转入一个干净的1.5ml离心管中,向吸附膜的中间部位悬空滴加50–100
μl经70℃水浴预热的洗脱缓冲液EB,室温放置2分钟,12,000 rpm(~13,000g)离心2分钟。
注: = 1 \* GB3 ① 洗脱缓冲液体积最好不少于50 μl,体积过小影响回收效率。
= 2 \* GB3 ② 洗脱液的pH值对于洗脱效率有很大影响。若用水做洗脱液应保证其pH值在7.0-8.5范围内,pH值低于7.0会降低洗脱效率。
13.
DNA产物-20℃保存。
大量操作步骤(针对含微量核酸的样品)
1. 称1-5
g土壤置于10ml离心管中,加入1gGlass Beads,再加入3ml
缓冲液R1与200μl
缓冲液R2。涡旋器高速震荡3-5分钟。
2.
加入600μl
缓冲液R3,涡旋混匀。70℃水浴处理10分钟。期间振荡几次。
3.3000g离心3分钟,转移上清到新的离心管中,加入550μl
缓冲液R4混匀。
4.
冰上放置5分钟。8000
g离心10分钟。转移上清到新的离心管中。
5.
以下按标准操作步骤的第五步继续操作。
● DNA浓度及纯度检测:
基因组DNA片段的大小与样品保存时间、操作过程中的剪切力等因素有关。提取的DNA片段可用琼脂糖凝胶电泳和紫外分光光度计检测浓度与纯度。可配制0.8-1.0%琼脂糖凝胶,使用λ/HindIII判断基因组的大小,完整的基因组大小应在23kb以上。使用分光光度计检测时, OD260/OD280比值应为1.7–1.9之间,如果洗脱时不使用洗脱缓冲液,而使用去离子水洗脱,比值可能偏低,但并不表明DNA纯度不高。
● 常见问题分析:
|
常见问题
|
可能原因
|
建议
|
|
没有洗脱出DNA
|
缓冲液R5没有加入异丙醇
|
样品过柱前,必须用异丙醇调整核酸结合条件,否则核酸不能挂柱。
|
|
漂洗缓冲液PW中没有加入乙醇
|
漂洗缓冲液PW使用前请按照标签加入无水乙醇。无水乙醇加入量不正确会导致核酸提取量大大降低。
|
|
低浓度的DNA量
|
缓冲液R2使用过量
|
按照步骤1加入适量缓冲液R2
|
|
洗脱体积太小
|
洗脱体积不能低于50μl,如洗脱体积太小,回收率将大大降低。
|
|
洗涤不恰当
|
漂洗缓冲液PW使用前请按照标签加入无水乙醇。无水乙醇加入量不正确会导致核酸提取量大大降低。
|
|
低A260/A280比率
|
蛋白污染
|
不要忽略步骤8中用漂洗缓冲液WB1冲洗吸附柱
|
|
洗脱液pH值不合适
|
确保使用的洗脱液pH在8.0以上,如低于8.0将导致DNA洗脱量过低。
|
|
下游应用不好
|
提取的DNA含盐量高
|
漂洗缓冲液PW使用前请按照标签加入无水乙醇。
|
|
提取的DNA含有乙醇
|
步骤11空甩柱子2分钟非常关键,彻底去除漂洗液中的乙醇。
|
|
抑制PCR反应
|
增加缓冲液R2用量,彻底去除腐殖酸等PCR抑制因子;步骤4中确保不要吸取到沉淀。
|
实验示例:
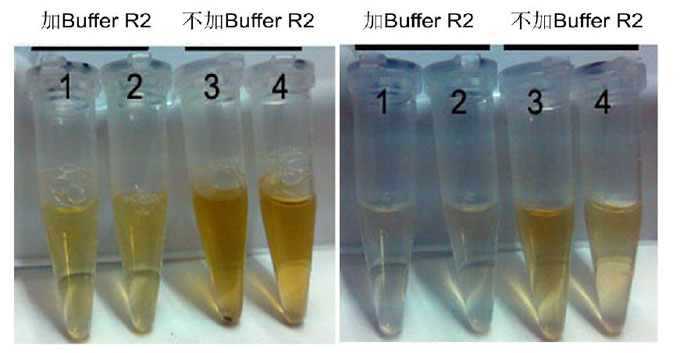
Buffer R2去除腐殖酸效果对比图
左图-步骤1提取时使用了Brffer R2,颜色明显浅很多(左1,左2),
说明Buffer R2对去除腐殖酸、色素等效果明显
右图-步骤3上清加入Buffer R4进一步处理,离心去除杂质,
裂解时加有Buffer R2的,再经Buffer R4处理几乎不再有颜色(右1,右2),
而不加Buffer R2的颜色还很深(右3,右4)。
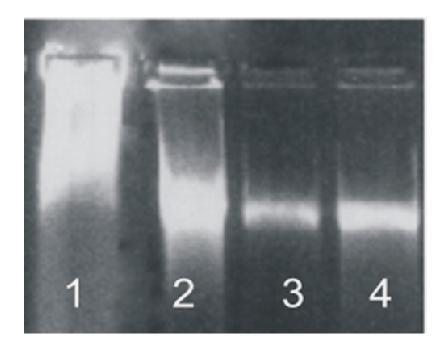
1, 2: SDS高盐酚氯仿抽提法
3, 4: 土壤基因组DNA提取试剂盒(RTG2403)提取
1, 3: 为花基土壤
2, 4: 河边淤泥